Düsseldorf/Kiel/Hamburg. Ein Forschungsteam der Christian-Albrechts-Universität zu Kiel (CAU) unter Beteiligung der Heinrich-Heine-Universität Düsseldorf (HHU) und der Universität Hamburg hat erstmals gezeigt, dass Tiefseeorganismen den problematischen Kunststoff PET mittels eines Enzyms abbauen können. Ihre Studienergebnisse stellen sie in der Fachzeitschrift Communications Chemistry vor und diskutieren dabei sowohl biotechnologische Anwendungen als auch die hohe Relevanz für biogeochemische Prozesse im Meer und an Land.
Plastikverschmutzungen beeinträchtigen zunehmend Küsten und Meere. Eines der Probleme sind Plastikflaschen, die aus dem Kunststoff Polyethylenterephthalat, kurz PET, hergestellt werden.
Forschende aus Kiel, Düsseldorf und Hamburg unter Leitung der CAU zeigten nun erstmals anhand von Mikroorganismen aus der Tiefsee, dass Polymere wie PET kontinuierlich durch ein Enzym in Tiefseeorganismen abgebaut werden können. Diese Ergebnisse erweitern grundlegend das Wissen über PET-abbauende Enzyme, den zugrundeliegenden Mechanismus sowie das evolutionäre Verständnis über die Vielfalt mutmaßlicher PET-abbauender Enzyme im gesamten globalen Ozean.
Erstmals wurde das PET-abbauende Enzym PET46 aus einem nicht-kultivierten Tiefsee-Mikroorganismus mit einem metagenomischen Ansatz – das genetische Material wird hierbei direkt aus Umweltproben gewonnen – identifiziert und biochemisch beschrieben. Dazu wurde das Gen aus einer Tiefseeprobe anhand von Ähnlichkeiten zu bekannten Sequenzen identifiziert, das entsprechend kodierende Gen synthetisiert, das Protein im Bakterium Escherichia coli hergestellt und anschließend biochemisch und strukturell untersucht.
PET46 besitzt viele ungewöhnliche Eigenschaften und erweitert den bekannten Bestand PET-abbauender Enzyme um einen fundamental neuen Bauplan. Strukturell unterscheidet sich das Enzym deutlich von bisher entdeckten Enzymen. Dadurch besitzt es die Fähigkeit, sowohl sehr langkettige PET-Moleküle, sogenannte Polymere, als auch kurzkettigere PET-Moleküle, sogenannte Oligomere, abzubauen, wodurch der Abbau kontinuierlich ablaufen kann.
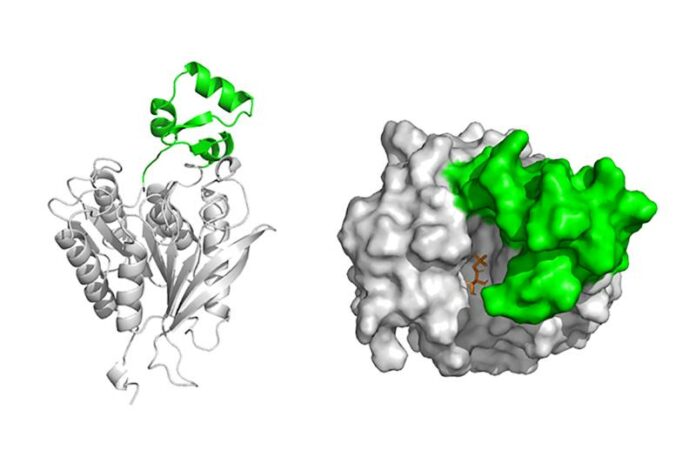
Dieses Enzym verwendet dabei unter anderem einen völlig anderen Mechanismus zur Substratbindung im Vergleich zu den bisher bekannten PET-abbauenden Enzymen. Das Forschungsteam beschreibt einen ungewöhnlichen ‚Deckel‘ aus 45 Aminosäuren oberhalb des aktiven Enzymzentrums als entscheidend für die Bindung. Bei anderen PET-Enzymen sind aromatische Aminosäuren nahe des aktiven Zentrums typisch.
Die Ergebnisse verdeutlichen eine Besonderheit des PET-abbauenden Enzyms PET46. „Wir haben in unserer Studie eine neue genetische Ressource aus Tiefseeorganismen aus dem Reich der Archaeen entdeckt“, sagt Prof. Dr. Ruth Schmitz-Streit von der CAU. Archaeen sind einzellige Organismen, eine von drei Domänen zellulärer Lebewesen neben den Bakterien und den Eukaryoten (Organismen mit Zellkern). Bisher bekannt waren etwa 80 verschiedene PET-abbauende Enzyme, die überwiegend in Bakterien oder Pilzen gefunden wurden. „Unsere Daten tragen dazu bei, das Wissen über die ökologische Rolle der Tiefsee-Archaeen und die mögliche Zersetzung von PET-Abfällen im Meer zu erweitern“, so die Mikrobiologin.
An der HHU wurde mittels Röntgenstrukturanalyse die dreidimensionale Struktur des Enzyms bestimmt. Prof. Dr. Sander Smits, Leiter des Center for Structural Studies (CSS): „Dies bedeutet, dass wir mit atomarer Auflösung die genaue Form des Enzyms feststellen konnten. So machten wir auch dessen ungewöhnlichen „Deckel‘ sichtbar.“ Die Existenz dieses Deckels konnte mit den üblichen computergestützten Methoden nicht vorhergesagt werden.
Die Arbeitsgruppe von Prof. Dr. Holger Gohlke (Institut für Pharmazeutische und Medizinische Chemie) hat aufbauend auf der von den Kollegen entschlüsselten Struktur im Computermodell ein kleines Stück PET-Kunststoff in das aktive Zentrum des Enzyms eingeführt. So fanden die Forschenden heraus, wie genau das Enzym an das PET-Stück bindet, um es abzubauen. Wenn dieser Mechanismus bekannt ist, kann das Enzym mit molekularbiologischen Methoden verändert werden, um den Abbauprozess zu optimieren. Prof. Gohlke: „Interessanterweise zeigte sich dabei, dass der ,Deckel´ in der Struktur in einer nicht-optimalen Orientierung für die PET-Bindung ist, was deutlich macht, wie sich die angewendeten Methoden gegenseitig ergänzen.“
Am HHU-Institut für Molekulare Enzymtechnologie auf dem Campus des Forschungszentrums Jülich wurden in der Arbeitsgruppe von Prof. Dr. Karl-Erich Jaeger Experimente zur biochemischen Charakterisierung des Enzyms vorgenommen.
Vielversprechende Anwendungen in der Biotechnologie
Auf molekularer Ebene weist PET46 große Ähnlichkeiten zu anderen Enzymen, den „Ferulasäure-Esterasen“, auf. Diese tragen zum Abbau des natürlichen Polymers Lignin aus Pflanzenzellwänden bei. Lignin und PET haben viele strukturelle Ähnlichkeiten, so dass Lignin-abbauende Enzyme möglicherweise auch für den Abbau des nicht-natürlichen Substrats PET in Frage kommen können.
Die biochemischen Eigenschaften von PET46 machen es damit sowohl biotechnologisch für den Abbau von Kunststoffen aus dem Meer und vom Land sehr interessant. Im Vergleich zu bisher beschriebenen PET-abbauenden Enzymen aus Bakterien und aus Kompostanlagen ist PET46 bei einer Temperatur von 70 Grad Celsius deutlich effizienter als andere Referenzenzyme bei deren jeweils optimalen Temperaturen.
Projekt PLASTISEA
Strukturbiologen, Bioinformatiker, organische Chemiker und Mikrobiologen an der HHU arbeiten in mehreren Verbundprojekten an der Erforschung von Lösungsansätzen rund um das Thema Plastikmüll. Partner sind hier zum Beispiel die Helmholtz-Zentren in Jülich, Leipzig und Kiel und die Universitäten in Aachen, Hamburg und Kiel. Die nun in Communications Chemistry beschriebenen Forschungsergebnisse sind im Projekt PLASTISEA entstanden, das von Prof. Dr. Ute Hentschel Humeida vom GEOMAR Helmholtz-Zentrum für Ozeanforschung Kiel koordiniert wird.
Die strukturbiologischen Untersuchungen an der HHU waren Bestandteil eines weiteren Projekts namens LipoBiocat. Die Projekte PLASTISEA und LipoBiocat wurden vom Bundesministerium für Bildung und Forschung in den Programmen „Neue biotechnologische Prozesse auf der Grundlage mariner Ressourcen – BioProMare” und „Maßgeschneiderte Inhaltstoffe 2“ gefördert (Förderkennzeichen: 161B0867D und 031B0837A).
Pressemitteilung der Universität Kiel.
Originalpublikation
Pablo Perez-Garcia, Jennifer Chow, Elisa Costanzi, Marno Gurschke, Jonas Dittrich, Robert F. Dierkes, Rebecka Molitor, Violetta Applegate, Golo Feuerriegel, Prince Tete, Dominik Danso, Stephan Thies, Julia Schumacher, Christopher Pfleger, Karl-Erich Jaeger, Holger Gohlke, Sander H. J. Smits, Ruth A. Schmitz & Wolfgang R. Streit, An archaeal lid-containing feruloyl esterase degrades polyethylene terephthalate. Commun Chem 6, 193 (2023)



























